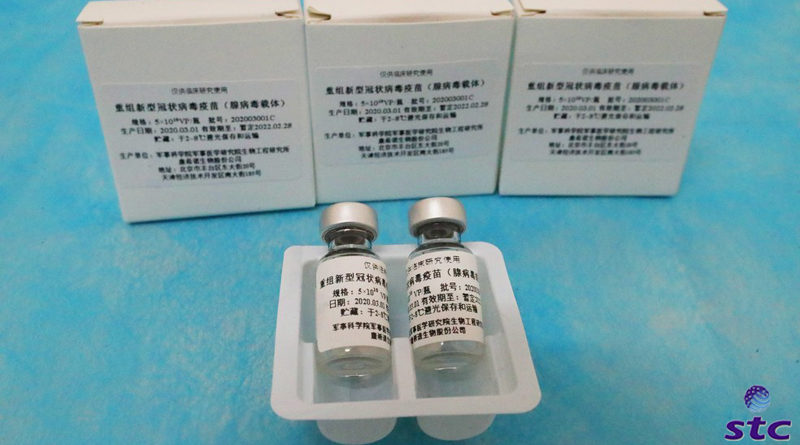
Anvisa deve responder até a próxima quarta (17) se autoriza uso da vacina da CanSino
A agência reguladora recebeu o pedido da farmacêutica chinesa ontem
A Agência Nacional de Vigilância Sanitária (Anvisa) recebeu, nesta quarta-feira (10), o pedido de autorização para uso emergencial da vacina Convidecia, produzida pelo laboratório chinês CanSino. Com a solicitação em mãos, o órgão tem sete dias úteis para analisá-la.
Assim, a resposta sobre a liberação ou não do imunizante deverá ser dada até a próxima quarta-feira (17 de novembro). O prazo, contudo, não considera o tempo para o laboratório responder aos questionamentos feitos pela agência no decorrer do processo.
Segundo a Anvisa informou em comunicado nesta quarta, nas primeiras 24 horas de análise, o processo foi submetido à triagem para análise sobre a documentação exigida.
Como a solicitação foi recebida ainda ontem pela agência reguladora, essa primeira etapa já será finalizada nesta quinta-feira (11).
O imunizante é aplicado em uma única dose. Em março, a farmacêutica chinesa já havia manifestado interesse em trazer a sua vacina contra a Covid-19 para o Brasil.
Houve, na época, uma reunião com a Anvisa para esclarecimento das normas e requisitos técnicos para pedidos de registro emergencial.
No Brasil, apenas a vacina Janssen — fabricada pela Johnson & Johnson — é de aplicação única.
- Prefeitura Municipal de Sobral apresenta à CDL serviços para a população em situação de rua - 19/06/2024
- Mais de 20 mil torcedores estão confirmados em jogo entre Ceará e Coritiba na Série B - 29/05/2024
- Casa da Economia Solidária comemora 10 anos com ações para grupos solidários e Feira Solário - 29/05/2024